アミノ酸とは
「アミノ酸」は化学式RCH(NH2)COOHで表される有機化合物であり、カルボキシ基(-COOH)とアミノ基(-NH2)及び側鎖(R)から成ります。天然には約500種類のアミノ酸が見つかっていますが、生物の体の構成成分であるタンパク質の基となるアミノ酸はその内たった22種類です。ヒトでは、さらに2種類少ない20種類のアミノ酸で、体をつくるタンパク質が構成されています。アミノ酸には様々な用途があり、ヒトにとって必須の栄養素になるだけでなく、非常に有用な化合物であると言えます。
ヒトの体をつくるアミノ酸20種類
|
バリン、イソロイシン、ロイシン、メチオニン、リジン(リシン)、フェニルアラニン、トリプトファン、スレオニン(トレオニン)、ヒスチジン、アルギニン、グリシン、アラニン、セリン、チロシン、システイン、アスパラギン、グルタミン、プロリン、アスパラギン酸、グルタミン酸 |
アミノ酸は生命の起源?
1953年、シカゴ大学のユーリーとミラーは、原子地球の状態を再現した密閉空間をつくりアミノ酸を含む様々な有機分子を合成することに成功しました。この結果から、アミノ酸の出現は、生命誕生の可能性を示唆するものであると考えられてきました。しかし、その後の研究では、アミノ酸は生命が誕生するよりも遥か以前に出現していたと報告されています。また、小惑星りゅうぐうから探査機「はやぶさ2」が持ち帰った砂には15種類のアミノ酸が含まれていたと発表されています。これは、隕石によってアミノ酸が地球にもたらされたという可能性を示唆する知見です。どのようにアミノ酸が地球上に出現したのか、そして出現したアミノ酸と生命誕生との関係解明には今後より多くの研究成果が待たれます。
(J Theoretical Biology, 2019: DOI: 10.1016/j.jtbi.2019.110097)
(Science, 2023: DOI: 10.1126/science.abn9033)
アミノ酸の分類
アミノ酸は、カルボキシ基(-COOH)とアミノ基(-NH2)をもつ化合物の総称であり、構造や性質などによって分類されます。カルボキシ基とアミノ基が同じ炭素に結合したアミノ酸をα-アミノ酸と呼びます。タンパク質を構成するアミノ酸は、プロリンを除き、すべてα-アミノ酸です。カルボキシ基が結合する炭素の1つ隣の炭素にアミノ基が結合するとβ-アミノ酸、2つ隣の場合はγ-アミノ酸と呼ばれます。このように、アミノ酸は、カルボキシ基とアミノ基の位置によって分類が異なります。
アミノ酸は化学的な構造によっても分類されます。アミノ酸は1つの炭素原子に、カルボキシ基、アミノ基、水素、側鎖(R)が結合しています。側鎖が水素であるグリシンを除き、炭素原子に4つの異なる分子が結合することになります。そのため、同じアミノ酸であっても光学異性体(鏡像異性体)という2つの異なる立体構造を取りうることになります。これらはL体、D体(またはL型、D型)と呼ばれており、L体とD体は構造が鏡合わせの関係になっています。タンパク質を構成するアミノ酸は、基本的にL-アミノ酸であるとされてきましたが、最近、細胞内にD-アミノ酸もあることがわかってきています。
タンパク質を構成する20種類のアミノ酸は構造による違いに加え、化学的な性質によっても分類されます。アミノ酸は水への親和性によって、疎水性アミノ酸と親水性アミノ酸に分けられます。この性質は、側鎖によって変わり、非極性側鎖を持つアミノ酸(グリシン、アラニン、バリン、ロイシン、イソロイシン、フェニルアラニン、トリプトファン、プロリン、メチオニン)は疎水性アミノ酸です。一方で、極性側鎖を持つアミノ酸(セリン、トレオニン、アスパラギン、グルタミン、チロシン、システイン、アルギニン、リシン、ヒスチジン、グルタミン酸、アスパラギン酸)は親水性アミノ酸です。また、塩基性側鎖を持つアルギニン、リシン、ヒスチジンは塩基性アミノ酸、酸性側鎖を持つグルタミン酸とアスパラギン酸は酸性アミノ酸と呼ばれています。残りの15個のアミノ酸は、中性アミノ酸です。
タンパク質をつくるアミノ酸
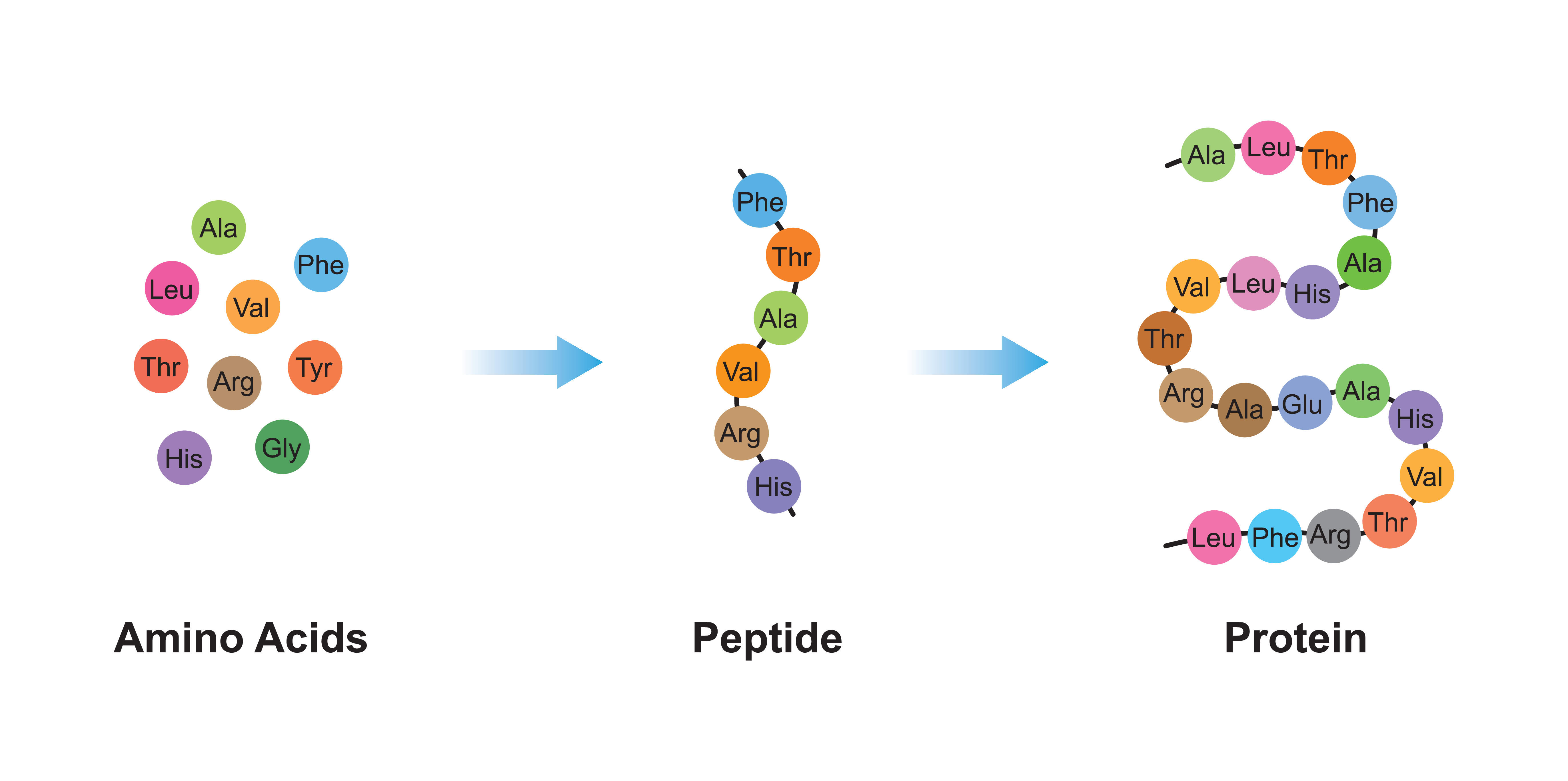
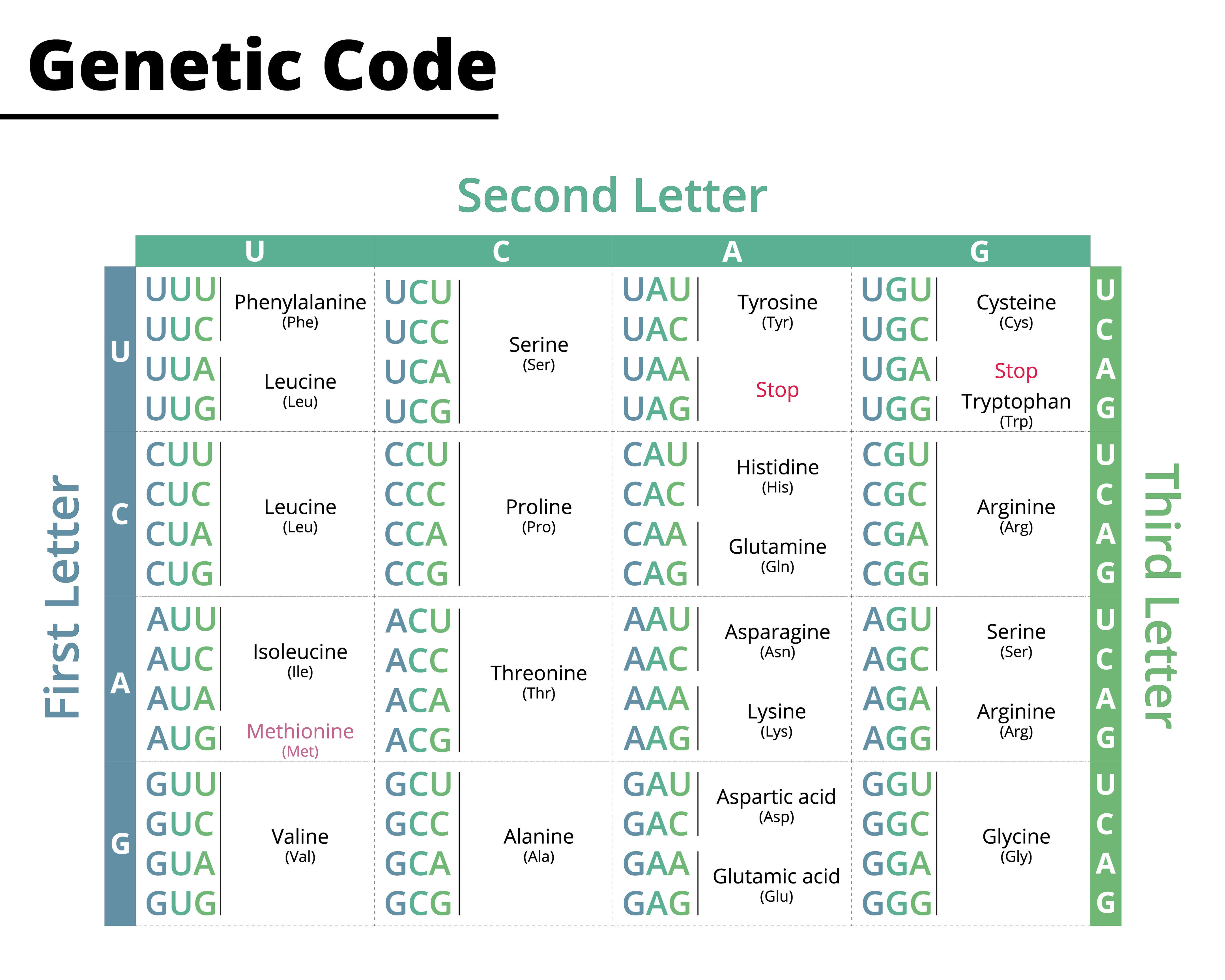
アミノ酸は、炭素、窒素、酸素、水素で構成され、硫黄を含むこともあります。アミノ酸は、細胞内ではアミノ酸分子やイオンとして存在するほか、アミノ酸同士が繋がってタンパク質を構成しています。アミノ酸同士の結合は、ペプチド結合(-CO-NH-)と呼ばれています。ペプチド結合は、一方のアミノ酸のカルボキシ基(-COOH)ともう一方のアミノ酸のアミノ基(-NH2)から、水分子(H2O)が取れることによって形成されます。ペプチド結合によってアミノ酸が重合している分子をポリペプチドと呼びます。このポリペプチドはタンパク質の基本構造となっており、20種類のアミノ酸の組合せや並び順によって、ヒトではおよそ10万種類ものタンパク質がつくられます。どのアミノ酸がどのような順番で結合するかは、遺伝子であるDNA及びその転写産物であるRNAによって決定されます。
その他のアミノ酸
タンパク質を構成するアミノ酸は20種類ですが、生物は他にも様々なアミノ酸を有しています。α-アラニンの構造異性体であるβ-アラニンは天然に存在し、ヒスチジンと結合してカルノシンというジペプチドを形成します。カルノシンは動物の筋肉中に多く存在し、脂質の抗酸化作用を持つとされています。また、L-アラニンの光学異性体であるD-アラニンは、細菌の細胞壁成分となることが知られています。他にも、L-セリンの光学異性体であるD-セリンは、哺乳動物の脳にあり、記憶や学習などの高次機能に関与することも知られています。
アミノ酸の異性体以外にも、様々な形で天然アミノ酸が存在します。生体にとってアンモニアは有害ですが、このアンモニアを尿素に変えて無毒化するのが尿素回路です。この尿素回路では、中間体としてオルニチンやシトルリンが生成されますが、これらの化合物もアミノ酸です。また、神経伝達物質として知られるγ-アミノ酪酸は、通称GABA(ギャバ)と呼ばれ、チョコレートなどにも入っているため、よく知られています。このGABAもアミノ酸です。他にもお茶に含まれる旨味成分であるテアニンもアミノ酸です。このように、アミノ酸には生理作用を有するものがたくさんあります。
必須アミノ酸と非必須アミノ酸
アミノ酸は、炭素と窒素を含む化合物であるため、細胞内の炭素や窒素の代謝に関わる化合物から合成されます。生物は、タンパク質をつくる22種類のアミノ酸をすべて合成できるわけではありません。進化の途上でタンパク質を構成するアミノ酸のおよそ半数を合成できなくなったと考えられています。どのアミノ酸を合成できて、どのアミノ酸を合成できないかは、その生物によります。
ヒトが自身の体内で合成できないアミノ酸は、そのアミノ酸を含むタンパク質を栄養として食物から摂取しなければなりません。このようなアミノ酸を必須アミノ酸、自分で合成できるアミノ酸を非必須アミノ酸と呼びます。ヒトは、イソロイシン、トリプトファン、トレオニン、バリン、ヒスチジン、フェニルアラニン、メチオニン、リシン、ロイシンを体内で合成できないため、この9種類が必須アミノ酸です。
アミノ酸の用途
アミノ酸は、以下に示す通り私たちの生活において欠かせない化合物となっています。
| 1. 医薬品原料 | アミノ酸自体が医薬品になるとともに、医薬品の原料ともなります。錠剤や顆粒だけでなく、輸液の成分としても使われます。 |
| 2. 医療食 | 病人など、栄養条件が不十分な人や、吸収力の低下したお年寄りの栄養補助として利用されます。 |
| 3. 健康食品 | 食事で不足するアミノ酸を補うために、健康食品としても販売されています。特に、アスリートの栄養補助によく使われています。 |
| 4. 食品、飲料 | うま味調味料などとして多く使われています。また、一般的な食品や飲料でも健康食品に準じた機能を付与するために使われています。 |
| 5. 化粧品 | アミノ酸が有する保湿性やpH調整能を利用するために、化粧品に使用されています。 |
| 6. 培地 | 研究開発では、細胞を培養して研究が進められていますが、この細胞培養のための培地に多く使われています。 |
| 7. 肥料・飼料 | 家畜の成長を促進するために使われています。また、養殖魚の健康維持や農作物の肥料にも使用されています。 |
アミノ酸の製造方法
さまざまな用途に使われるアミノ酸ですが、どうやって合成するのでしょうか?天然アミノ酸の中には重要な生理活性を持つものが数多く存在し、また、医薬品としてD体または非天然型のアミノ酸が数多く使われています。このため、アミノ酸の合成(特に不斉合成)は需要が高く、種々の方法が提案されています。アミノ酸の製造方法には、発酵法、酵素法、抽出法、化学合成法などがあります。
古くから用いられているアミノ酸の合成法として、 ストレッカー合成があります。文字通りストレッカー反応を利用した方法で、アルデヒドとアンモニア、シアン化水素の3成分縮合によってα-アミノニトリルを合成し、この加水分解によりアミノ酸を得るという方法です。この方法ではアンモニアとして塩化アンモニウムを用いますが、塩化アンモニウムの代わりにキラルなアミンを用いることで、片方の片方の光学異性体を主生成物として得ることができます。この方法は不斉ストレッカー法と呼ばれています。
工業的には、微生物を用いたアミノ酸発酵法によって大量に合成されています。人工的に突然変異させた微生物株を、炭素源となる糖類や窒素源となる硫酸アンモニウムと共に培養することで、安価に目的のアミノ酸が合成できます。アミノ酸の発酵法による製造は、1950年代に、グルタミン酸を細胞外に排出するコリネ型細菌が単離されたことで発展してきました。コリネ型細菌を使ったアミノ酸発酵は日本の研究者らによって発見され、現在においてもアミノ酸製造の主要な方法として確固たる地位を築いています。
この他にも、アミノ酸の前駆体(アミノ酸に近い化合物)まで合成したのち、酵素を反応させて目的のアミノ酸をつくる酵素法や、タンパク質を分解してアミノ酸をつくる抽出法などもあります。
まとめ
アミノ酸はアミノ基とカルボキシ基の両方を持つ化合物の総称であり、構造や化学的な性質で分類されています。200年以上前に見つかったアミノ酸ですが、自然界には500種類を超えるアミノ酸が存在することがわかっています。こうした天然のものや非天然型のものも含め医薬品から食品、化粧品や肥料・飼料まで様々な用途で使われています。このため、化学合成法や発酵法などの方法によって、工業的に大量生産されているものもあります。このように、人間社会に欠かせない重要な化合物であるアミノ酸は、現在でも幅広く研究開発が進められています。
<参考文献>
今堀和友,山川民夫 監. 生化学辞典. 第4版, 東京化学同人, 2007, 1632p.
田宮信雄,八木達彦 訳. コーン・スタンプ生化学. 第5版, 東京化学同人,1988, 652p.
Lisa A. Urry, Michael L. Cain. et al. Campbell Biology, 11th ed., Pearson, 2016, 1488p.
<参考サイト>
協和発酵バイオ株式会社HP
味の素株式会社HP
(上記すべて参照:2023-5-29)