リケラボは研究者、研究開発・技術職など理系の知識を生かしてはたらきたい人を応援する情報サイトです。

次世代の画期的な医療として、iPS細胞を使った再生医療が注目を集めています。iPS細胞の特徴は次の2点。ほぼ無限に増殖可能なことと、理論上どのような細胞もつくり出せること。ただ、無限増殖が可能とはいえ、現状は細胞培養を人手に頼っているため、大量生産は難しいのが現状です。そんな中、iPS細胞を使った血小板の大量生産に挑戦しているのが、京都大学iPS細胞研究所(CiRA)の江藤浩之教授です。江藤教授に血小板製造研究の現状と今後の見通し、先生ご自身の研究者としての歩みなどを伺いました。
50年後にあるべき医療を想定し、今できることに取り組む
そもそも血小板とは、どのような役割を担っているのでしょうか。
血小板は血液成分の一つであり、血液を固まらせて止血する機能がよく知られますが、他にもいくつもの重要な役割があります。例えば近いところでは、米大リーグ、エンゼルスの大谷翔平投手がPRP注射(プレートレット・リッチ・プラズマ=多血小板血漿)を行ったという報道もありました。PRP注射は自分の体内から採取した血小板を集めて患部に注入します。これにより自己修復力を高めて、部分断裂した靭帯の回復を促すのです。血小板はほかにも、栄養や薬の運搬機能などを備えています。
病気の治療などに使われる血小板製剤は、献血により作られているのですね。
そのとおりです。ただし、献血によってつくられる現在の血小板製剤には保存期間の問題があります。製剤の有効期間が、日本では4日、アメリカでは5日と極めて短いのです。そのためアメリカでは、血小板製剤の約18%が廃棄されているとする報告もあります。一方で献血だけに頼る現状のシステムを今後も続けていて良いのか、というのが私の問題意識です。50年後の医療のあるべき姿を考えるなら、献血以外の方法も考えておくべきでしょう。人口減少社会に突入した日本では、今後必要なだけの献血者を確保できなくなる恐れもあります。そのときになってあわてるようではいけません。
■iPS細胞から血小板をつくる
iPS細胞を使って血小板を作る際の課題は何でしょうか。
実際の治療を考えるなら、膨大な量の血小板が必要になることです。血小板は、巨核球から産生され核を持ちません。その大きさは約2μmであり、赤血球や白血球よりもかなり小さな細胞です。ただ小さいだけに血中には大量に含まれており、1μLあたり15~40万個含まれています。
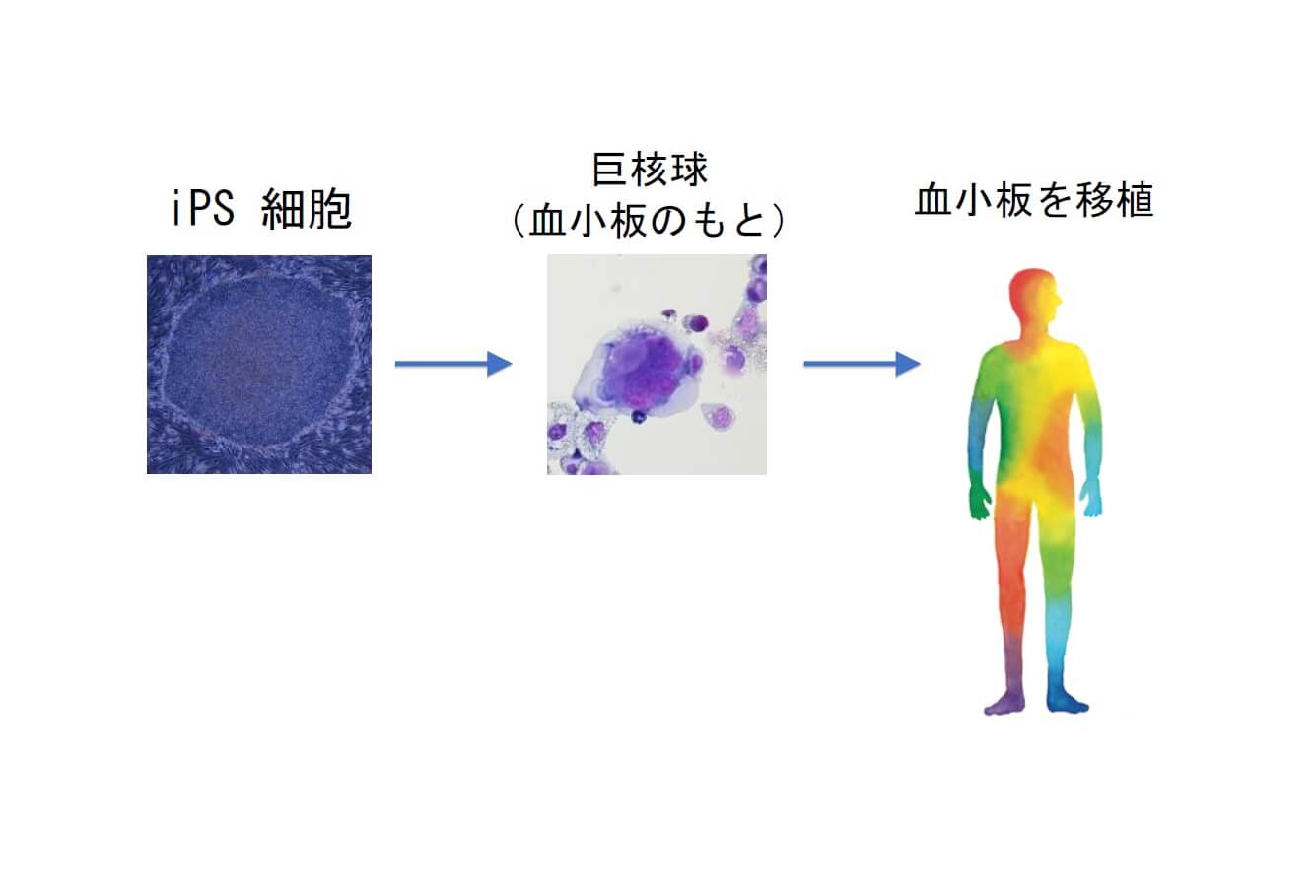
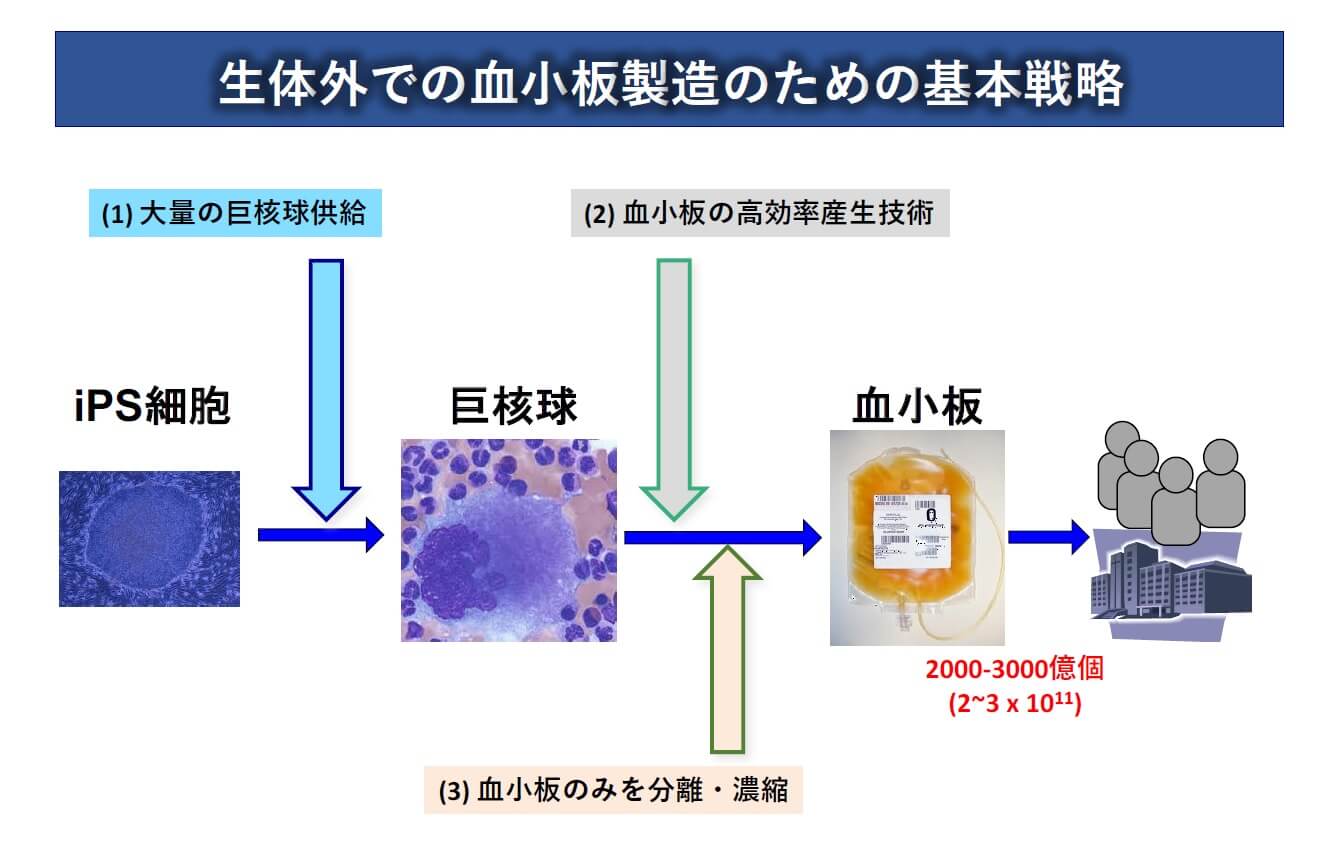
iPS細胞から血小板を作る場合には、まずiPS細胞から巨核球を作り、巨核球から血小板を作る2段階のプロセスが必要です。その場合にいくつかクリアすべき課題がありますが、最大のハードルとなるのは数です。血小板製剤として治療に使う場合、1回あたり2000~3000億個の血小板が必要です。この数は、ほかの再生医療として知られる網膜再生の際に使われる網膜色素上皮細胞の約1万個、パーキンソン病治療に必要なドーパミン産生神経細胞の約500万個とくらべてもケタ違いに多いのです。
それほど大量の血小板をどのようにつくるのでしょう。
大量生産は、次の3つのステップで実現します。まずiPS細胞から大量の巨核球をつくり、続いて巨核球から血小板を高効率に産生し、最後に血小板のみを分離・濃縮します。文章では、このように簡潔にまとめられますが、実際のプロセスは決して簡単なものではなく、開発をスタートしてから既に7年が経過しています。それでもようやく大量生産のメドが立ち始めたのが現状です。
血小板を大量生産する際の一番の問題はなんですか。
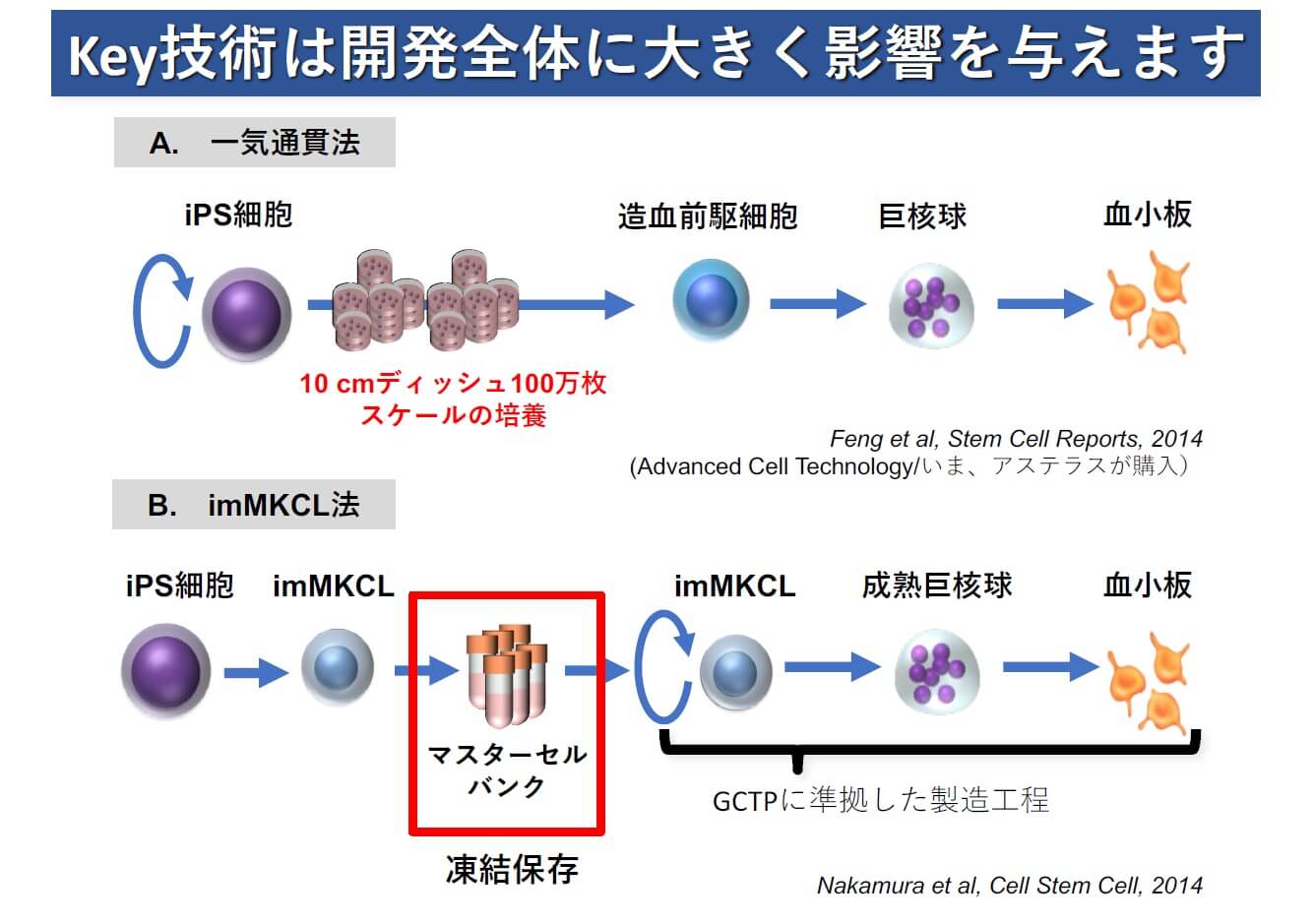
iPS細胞を使った再生医療では、一気通貫でiPS細胞から最終的に移植する細胞を作る方法がとられるケースが多く見られます。血小板に当てはめるなら、保存しておいたiPS細胞から造血前駆細胞を培養し、それを巨核球へと分化させ、巨核球を成熟させて血小板を放出させるところまで、途中で中断することなく生産するのです。血小板をこの方法で作製しようとすると、iPS細胞を大量に培養する必要があります。仮に10センチの培養皿を使うとすれば、100万枚単位での培養が必要です。iPS細胞を大量に増殖させる過程では、作業者や場所、条件によってiPS細胞の品質にばらつきが生じるため、現実問題としてiPS細胞を原料とした一気通貫での血小板の大量生産は不可能です。
手作業の限界を打ち破る方法で特許を取られたのですね。
大量生産を実現するために開発したのが、不死化巨核球株(immortalized megakaryocyte progenitor cell line:imMKCL)を原料とする方法です。imMKCLは、iPS細胞を造血多能性前駆細胞に分化させた段階で、巨核球の増殖、細胞老化の抑制、細胞死の抑制を図る3つの遺伝子を導入してつくります。これによりimMKCLは、自己複製能を獲得して活発に増殖する。このimMKCLを操作すると血小板を放出するようになるのです。imMKCLは凍結保存が可能であるため、大量に保存しておいて必要に応じて解凍・培養して血小板をつくれば、短期間での大量生産が可能となります。
iPS細胞から血小板を作る技術は安全性に関しても、2つの優位性を備えています。一つには献血による輸血につきものの細菌やウイルス感染などのリスクがないことです。マスター細胞の安全性を確保し、厳密に無菌管理した状態で血小板をつくるため病原リスクをほぼなくすことができます。もう一点は、iPS細胞による再生医療で懸念される点であるガン化のリスクがないこと。血小板自体は核を持たないため増殖能力がなく、製剤プロセスで放射線照射をするため、ガン化リスクはありません。
現在、開発はどこまで進んでいるのでしょうか。
成熟巨核球の大量生産はクリアし、今は第2ステップの巨核球からの血小板の高効率産生がほぼ見えてきた段階です。とにかく、ヒトに入れる前提で研究を進めているので、高効率産生での品質確保が最重要課題です。ヒトに投与できる品質の血小板を、再現性を持って作れること。コストも踏まえるなら材料も、可能な限り安価な材料、画期的な材料を使いたい。実用化のためには、コストダウンも考慮する必要があり、これについても研究室の別のチームが研究に取り組んでいます。

▲細胞培養室で細胞の状態を確認するために顕微鏡をのぞく研究者/提供:京都大学iPS細胞研究所
臨床医から研究者へ、転機となったアメリカ留学
江藤先生は最初、循環器内科の臨床医を務められていたと伺いました。
心筋梗塞や狭心症の患者さんに対するカテーテル治療を、ほとんど毎日、それも病院に泊まり込むような感じでやっていました。若い頃から馬力だけは自信がありましたから。ところが医局の都合もあって、私にアメリカ留学のチャンスが回ってきました。とはいえ、それまで細胞培養や分子生物学などの研究をしたことなど一度もなかったので、留学当初は具体的な目的など何もありませんでした。
それでも結局は研究に取り組まれたのですね。
1年の約束でしたから、せっかくなら論文を書こうと一念発起し、また馬力にものを言わせてがんばりました。朝から仕事して、お弁当を食べたら机で仮眠して、夕方まで働いて家で晩ごはんを食べたら、もう一度研究室に戻って夜中まで働く。研究所の前がゴルフ場だったので、朝は5時起きで1ラウンドまわって、頭を空っぽにしてから、その日の研究に取りかかる。愚直にハードワークを続けたおかげで、4月からの8カ月で論文が完成し、2月に受理されたのです。また、ボスがフェローシップを申請しろというので、書類を出したら運良く通ってしまいました。
留学助成金を得たので、続けて研究されたのですか。
とりあえずもう2年間、大学を休職させてもらって、本格的に研究に向き合ってみようと血小板の研究に取り組みました。循環器内科にとって血小板は、心筋梗塞や脳梗塞を引き起こす厄介な存在です。とはいえ血液内科や小児科の先生にとっては、極めて重要な存在でもある。血小板についての基礎研究に取り組み、2年後に今度はグラントつまり研究費を取れるレベルだとボスに言われて、申請書を出したら、また通ってしまった。これをキッカケに思いきって研究者に転身する覚悟を決めたのです。
研究対象はやはり血小板ですか。
ちょうどその頃から、遺伝子操作が実用段階に入りつつありました。ES細胞を使って遺伝子操作したマウスを作り、血小板の機能を調べていました。そこで血小板の研究をするなら、わざわざマウスをつくらずとも、マウスのES細胞から直接、遺伝子操作した血小板をつくれないかとチャレンジしたところ、悪戦苦闘の末にできたのです。これは世界で初めて、ES細胞から血小板をつくった論文として注目を集めました。この論文が東京大学医科学研究所におられた中内啓光教授(現・スタンフォード大学医学部教授)の目にとまり、私をスカウトしてくださったのです。
東京大学を経てiPS細胞研究所(CiRA)に移られたのですね。
東京大学では6年間で、サルのES細胞、そしてヒトのES細胞を使ってそれぞれの血小板をつくっています。2007年に山中先生のiPS細胞が発表されたので、iPS細胞でも血小板をつくり論文を出したところ、山中先生からCiRAに来ないかと誘ってもらったのです。その後、iPS細胞を使った血小板製剤の開発に取り組むベンチャー企業、株式会社メガカリオンのアドバイザーに中内先生と共になり、2017年からは千葉大学再生治療学研究センターでも教授を務めています。こうして自分の人生を改めて振り返ってみると、いつも誰かに引っ張ってもらってきためぐり合わせに感謝するしかありません。

▲オープンラボで実験を行う様子/提供:京都大学iPS細胞研究所
■イノベーター集団の中で異彩を放つ
先生の研究は独創的で、iPS細胞による再生医療に新たな方法論を提供されたのではないでしょうか。
従来の一気通貫法とは異なる手法を開発できたのは、単純に「ヒトに入れる」ためにどうすればよいかを突き詰めた結果です。iPS細胞でも主流は、自家移植ではなく他家移植へとシフトしてきていますが、その先の実用化を考えるなら、細胞の自動培養が必須の課題です。培養を熟練技術者の手技に頼らなければならないようでは、細胞の量産は望むべくもありません。量産できなければ、コストが下がらないため、再生医療の恩恵を受けられる患者さんが限られてしまう。多くの患者さんを救うためには、ビジネス化も必須の課題といえます。
研究者としての今後のテーマを教えてください。
まずは血小板製剤の大量生産に、一刻も早くメドをつけることです。その次に取り組みたいのが、巨核球の謎の解明です。巨核球自体は、まだまだわからないことだらけであり、それは裏返せば巨核球をほかの治療用途に使える可能性を意味します。アイデアはいろいろ温めているので、できる限り早く新しい研究をスタートさせたい。次の研究ではおそらく、進化したAIが大きく役に立つと期待しています。
研究者ほど素晴らしい仕事はない
研究者をめざす若者にメッセージをお願いします。
はっきり言って、研究職ほどよい仕事は、この世に他にありません。決してオーバーではなく、素直にそう思います。まったく自由にものを考えることができ、自分の時間を思いのままに使えて、世界中の研究者たちと自由にディスカッションできるのです。もちろん、研究がうまく行かず苦しいときも多々ありますが、そもそも研究とは99.99%失敗するものです。けれども、失敗するからどうすればダメなのかを学べます。たとえ成功しなくとも少しは確実に前進しているのだから、失敗も楽しめばよいのです。ただ大切なのは失敗しても諦めないこと。その先には必ず成功が待っているはずです。

京都大学iPS細胞研究所 教授
千葉大学大学院医学研究院 先端研究部門 イノベーション再生医学 教授
江藤浩之(えとう・こうじ)
1990年3月、山梨医科大学医学部(現・山梨大学医学部)卒業、1996年4月、帝京大学医学部内科循環器グループ助手、1999年5月、米国Scripps研究所博士研究員、2003年1月、同・上級博士研究員。2003年11月、東京大学医科学研究所 ヒト疾患モデル研究センター 幹細胞治療(高次機能)研究分野助手、2008年4月、東京大学医科学研究所 幹細胞治療研究センター幹細胞治療部門 助教、2009年1月同センター ステムセルバンク特任准教授(PI: 独立研究者)を経て、2011年7月より京都大学iPS細胞研究所 教授、2016年9月より千葉大学大学院医学研究院イノベーション再生医学 教授併任。
(※所属などはすべて掲載当時の情報です。)
*再生医療に関わる仕事にご興味のある方はぜひChall-edge(チャレッジ)へご相談ください!
再生医療に関わるお仕事はコチラ! 再生医療求人一覧
関連記事Recommend
-

独自のバイオインフォマティクス技術で、世界を変える酵素をデザインする
株式会社digzyme 代表取締役CEO 渡来 直生
-

スキンケアの疲労回復効果を検証!日常に取り入れる「疲労の科学」
~大阪公立大学健康科学イノベーションセンター~
-

「子どもたちを心臓の再手術から救いたい」――。思いを叶えるために根本教授が採ったユーザーイノベーション戦略
心・血管修復パッチ「シンフォリウム®」開発のキーマンに聞く「医師にしかできないサイエンス」とは
-

iPS細胞の実用化に向けた挑戦
京都大学iPS細胞研究財団
-

栄養学の新潮流「時間栄養学」とは? 私たちの健康を左右する、食事と体内時計の密接な関係に迫る!
-

次のパンデミックに備え、社会により貢献できる研究を目指して 慶應義塾大学医学部 感染症学教室 南宮 湖
臨床と研究をつなぎ国際保健に活かす「フィジシャン・サイエンティスト」を実践
-

CRISPR-Cas9の精度を飛躍的に高める「セイフガードgRNA」を開発した、九州大学川又助教の発想法
-

折り紙技術を駆使して宇宙から血管、さらに細胞にも活用。いつも自分で道を切り開いて歩み続ける研究者、繁富(栗林)准教授
-

「一回の決断で人生は終わるわけではない」
イスラエルのフードテック企業で活躍する杉崎麻友さん- 広がる研究キャリアの選択肢 -
-

日本のライフサイエンスを世界へ!
スタートアップ支援から街づくりまで、研究を強力にバックアップするサイエンスコンシェルジュとは― 三井不動産 三井リンクラボ ―